El calor (representado con la letra Q) es la energía transferida de un sistema a otro (o de un sistema a sus alrededores) debido en general a una diferencia de temperatura entre ellos. El calor que absorbe o cede un sistema termodinámico depende normalmente del tipo de transformación que ha experimentado dicho sistema.
Dos o más cuerpos en contacto que se encuentran a distinta temperatura alcanzan, pasado un tiempo, el equilibrio térmico (misma temperatura). Este hecho se conoce como Principio Cero de la Termodinámica.
Hasta el siglo XIX se explicaba el efecto del ambiente en la variación de la temperatura de un cuerpo por medio de un fluido invisible llamado calórico. Este se producía cuando algo se quemaba y, además, que podía pasar de un cuerpo a otro. La teoría del calórico afirmaba que una sustancia con mayor temperatura que otra, necesariamente, poseía mayor cantidad de calórico.
Benjamin Thompson y James Prescott Joule establecieron que el trabajo podía convertirse en calor o en un incremento de la energía térmica determinando que, simplemente, era otra forma de la energía.
Un aspecto del calor que conviene resaltar es que los cuerpos no almacenan calor sino energía interna. El calor es por tanto la transferencia de parte de dicha energía interna de un sistema a otro, con la condición de que ambos estén a diferente temperatura. Sus unidades en el Sistema Internacional son los julios (J)
La expresión que relaciona la cantidad de calor que intercambia una masa m de una cierta sustancia con la variación de temperatura Δt que experimenta es:

CALOR ESPECIFICO
El calor específico (o capacidad calorífica específica) es la energía necesaria para elevar en un 1 grado la temperatura de 1 kg de masa. Sus unidades en el Sistema Internacional son J/kg K.
En general, el calor específico de una sustancia depende de la temperatura. Sin embargo, como esta dependencia no es muy grande, suele tratarse como una constante. En esta tabla se muestra el calor específico de los distintos elementos de la tabla periódica y en esta otra el calor específico de diferentes sustancias.
Cuando se trabaja con gases es bastante habitual expresar la cantidad de sustancia en términos del número de moles n. En este caso, el calor específico se denomina capacidad calorífica molar C. El calor intercambiado viene entonces dado por:
En el Sistema Internacional, las unidades de la capacidad calorífica molar son J/molK.
el calor absorbido por un cuerpo será positivo y el calor cedido negativo.
TABLA DE CALOR ESPECIFICO

Capacidad calorífica de un gas ideal
Para un gas ideal se definen dos capacidades caloríficas molares: a volumen constante (CV), y a presión constante (Cp).
CV: es la cantidad de calor que es necesario suministrar a un mol de gas ideal para elevar su temperatura un grado mediante una transformación isócora.
Cp: es la cantidad de calor que es necesario suministrar a un mol de gas ideal para elevar su temperatura un grado mediante una transformación isóbara.
El valor de ambas capacidades caloríficas puede determinarse con ayuda de la teoría cinética de los gases ideales. Los valores respectivos para gases monoatómicos y diatómicos se encuentran en la siguiente tabla:
donde R es la constante universal de los gases ideales, R = 8.31 J/mol K
Calor latente de un cambio de fase
Cuando se produce un cambio de fase, la sustancia debe absorber o ceder una cierta cantidad de calor para que tenga lugar. Este calor será positivo (absorbido) cuando el cambio de fase se produce de izquierda a derecha en la figura, y negativo (cedido) cuando la transición de fase tiene lugar de derecha a izquierda.
El calor absorbido o cedido en un cambio de fase no se traduce en un cambio de temperatura, ya que la energía suministrada o extraída de la sustancia se emplea en cambiar el estado de agregación de la materia. Este calor se denomina calor latente.
Latente en latín quiere decir escondido, y se llama así porque, al no cambiar la temperatura durante el cambio de estado, a pesar de añadir calor, éste se quedaba escondido sin traducirse en un cambio de temperatura.
Calor latente (L) o calor de cambio de estado, es la energía absorbida o cedida por unidad de masa de sustancia al cambiar de estado. De sólido a líquido este calor se denomina calor latente de fusión, de líquido a vapor calor latente de vaporización y de sólido a vapor calor latente de sublimación.
El calor latente para los procesos inversos (representados en azul en la figura anterior) tienen el mismo valor en valor absoluto, pero serán negativos porque en este caso se trata de un calor cedido.
En el Sistema Internacional, el calor latente se mide en J/kg.
La cantidad de calor que absorbe o cede una cantidad m de sustancia para cambiar de fase viene dada por:
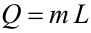
Este calor será positivo o negativo dependiendo del cambio de fase que haya tenido lugar.
TRANSMISIÓN DE CALOR

CONDUCCIÓN TÉRMICA
Es un proceso de transmisión de calor basado en el contacto directo entre los cuerpos, sin intercambio de materia, por el que el calor fluye desde un cuerpo de mayor temperatura a otro de menor temperatura que está en contacto con el primero. La propiedad física de los materiales que determina su capacidad para conducir el calor es la conductividad térmica. La propiedad inversa de la conductividad térmica es la resistividad térmica, que es la capacidad de los materiales para oponerse al paso del calor.
La transmisión de calor por conducción, entre dos cuerpos o entre diferentes partes de un cuerpo, es el intercambio de energía interna, que es una combinación de la energía cinética y energía potencial de sus partículas microscópicas: moléculas, átomos y electrones. La conductividad térmica de la materia depende de su estructura microscópica: en un fluido se debe principalmente a colisiones aleatorias de las moléculas; en un sólido depende del intercambio de electrones libres (principalmente en metales) o de los modos de vibración de sus partículas microscópicas (dominante en los materiales no metálicos).1
Para el caso simplificado de flujo de calor estacionario en una sola dirección, el calor transmitido es proporcional al área perpendicular al flujo de calor, a la conductividad del material y a la diferencia de temperatura, y es inversamente proporcional al espesor

Los materiales pueden ser conductores o aislantes.
CONVECCION:
La convección es una de las tres formas de transferencia de calor y se caracteriza porque se produce por medio de un fluido (líquido o gas) que transporta el calor entre zonas con diferentes temperaturas. La convección se produce únicamente por medio de materiales la evaporación del agua o fluidos. Lo que se llama convección en sí, es el transporte de calor por medio del movimiento del fluido, por ejemplo: al trasegar el fluido por medio de bombas o al calentar agua en una cacerola, la que está en contacto con la parte de abajo de la cacerola se mueve hacia arriba, mientras que el agua que está en la superficie, desciende, ocupando el lugar que dejó la caliente.
La transferencia de calor implica el transporte de calor en un volumen y la mezcla de elementos macroscópicos de porciones calientes y frías de un gas o un líquido. Se incluye también el intercambio de energía entre una superficie sólida y un fluido o por medio de una bomba, un ventilador u otro dispositivo mecánico (convección mecánica, forzada o asistida).
En la transferencia de calor libre o natural un fluido es más caliente o más frío y en contacto con una superficie sólida, causa una circulación debido a las diferencias de densidades que resultan del gradiente de temperaturas en el fluido.

RADIACCION:
emitida por un cuerpo debido a su temperatura. Todos los cuerpos emiten radiación electromagnética, siendo su intensidad dependiente de la temperatura y de la longitud de onda considerada. En lo que respecta a la transferencia de calor la radiación relevante es la comprendida en el rango de longitudes de onda de 0,1µm a 100µm, abarcando por tanto parte de la región ultravioleta, la visible y la infrarroja del espectro electromagnético.
La materia en un estado condensado (sólido o líquido) emite un espectro de radiación continuo. La frecuencia de onda emitida por radiación térmica es una función de densidad de probabilidad que depende solo de la temperatura.
Los cuerpos negros emiten radiación térmica con el mismo espectro correspondiente a su temperatura, independientemente de los detalles de su composición. Para el caso de un cuerpo negro, la función de densidad de probabilidad de la frecuencia de onda emitida está dada por la ley de radiación térmica de Planck, la ley de Wien da la frecuencia de radiación emitida más probable y la ley de Stefan-Boltzmann da el total de energía emitida por unidad de tiempo y superficie emisora (esta energía depende de la cuarta potencia de la temperatura absoluta).
A temperatura ambiente, vemos los cuerpos por la luz que reflejan, dado que por sí mismos no emiten luz. Si no se hace incidir luz sobre ellos, si no se los ilumina, no podemos verlos. A temperaturas más altas, vemos los cuerpos debido a la luz que emiten, pues en este caso son luminosos por sí mismos. Así, es posible determinar la temperatura de un cuerpo de acuerdo a su color, pues un cuerpo que es capaz de emitir luz se encuentra a altas temperaturas.
COMO:
-La radiación infrarroja de un radiador doméstico común o de un calefactor eléctrico es un ejemplo de radiación térmica.
-La luz emitida por una lámpara incandescente. La radiación térmica se produce cuando el calor del movimiento de partículas cargadas dentro de los átomos se convierte en radiación electromagnética.

CAMBIO DE FASE
de estado sólido a líquido, llamado fusión,
de estado líquido a sólido, llamado solidificación,
de estado líquido a gaseoso, llamado evaporación o vaporización,
de estado gaseoso a líquido, llamado condensación,
de estado sólido a gaseoso, llamado sublimación progresiva,
de estado gaseoso a sólido, llamado sublimación regresiva o deposición,
de estado gaseoso a plasma, llamado ionización.
de estado plasma a gaseoso, llamado Desionización




